课程邮箱 :shwyychyh@163.com 技术支持:武汉云思达科技

最全总结:国产PD-1百花齐放,中国肿瘤治疗或将进入“免疫治疗”时代
来源:admin 浏览量: 更新时间:2019-09-12 15:04:25
追本溯源,2013年,百时美施贵宝和默沙东分别公布了各自的PD-1药物O药(Opdivo,纳武利尤单抗)、K药(Keytruda,帕博利珠单抗)的临床试验结果:在已有治疗方案都无效的晚期转移性黑色素瘤患者中,O药、K药让60%的患者的肿瘤缩小乃至消失了超过2年!
这是PD-1抗体的首次露面,不鸣则已,一鸣惊人!
自此,PD-1一路披荆斩棘,大放异彩,在黑色素瘤、非小细胞肺癌、头颈部肿瘤等多个癌种中找到突破口,并成为首个跻身肺癌一线治疗的免疫治疗药物。
今年公布的最新数据也证实了K药、O药在当前非小细胞肺癌治疗中的卓越地位,长期生存数据显示:K药治疗初治患者的5年中位总生存率为23.2%,经治患者的5年中位总生存率为15.5%;O药治疗经治患者的4年总生存率为14%,对比化疗组(多西他赛)的5%的总生存率明显优异。
2018年6月15日,百时美施贵宝的O药正式获批进入中国市场,2018年7月25日,默沙东的K药也正式获批在中国上市,两大免疫“抗癌神药”在中国的正式亮相,宣告中国肿瘤免疫治疗拉开了序幕。
在O药、K药逐渐占据了免疫治疗领域的半壁江山时,国内各大药企也不甘示弱,纷纷加快研发进程,希望能在免疫治疗领域占得一席之地。
截至目前,国内已上市或已申报上市的PD-1/PD-L1药物共6种,除了O药、K药,其余四种皆为国产药物,其他还有大约10余种国产PD-1/PD-L1药物正在进行临床,国产PD-1/PD-L1药物大爆发,究竟能带来什么?一起来看看!
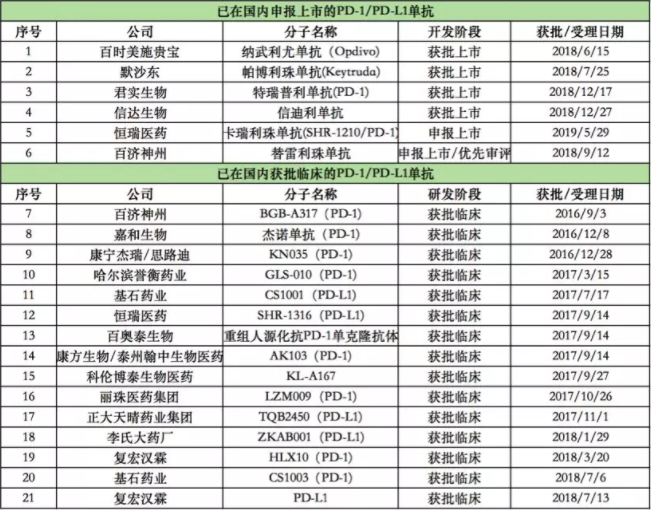
(部分信息来自GBI SOURCE)
(部分数据来源网络:国内已上市PD-1一览表)
1.信迪利单抗(达伯舒®)
制药公司:信达生物
(图片来源:信达生物官网)
达伯舒®(信迪利单抗注射液)是一种重组全人源抗PD-1 单克隆抗体,能特异性结合T细胞表面的PD-1分子,从而阻断导致肿瘤免疫耐受的 PD-1/程序性死亡受体配体 1(Programmed Cell Death-1 Ligand-1, PD-L1)通路,重新激活淋巴细胞的抗肿瘤活性从而达到治疗肿瘤的目的。
2018年12月27日,国家药品监督管理局正式批准信达生物制药与礼来制药共同开发的创新肿瘤药物PD-1抑制剂达伯舒®(信迪利单抗注射液)上市,用于至少经过二线系统化疗的复发或难治性经典型霍奇金淋巴瘤的治疗。
重点来了,信迪利单抗对比两大“抗癌神药”O药、K药究竟疗效如何?
研究数据显示:对于复发/难治性经典型霍奇金淋巴瘤,在6个月PFS(无进展生存期)上,信迪利单抗VS O药为77.6% VS 77%,信迪利单抗VS K药为77.6% VS 69%,效果相近。
但在ORR(客观缓解率)上,信迪利单抗的ORR接近80%,O药为65%,K药为69%,可以看到,信迪利单抗是优于O药、K药的。
由此可见,信迪利单抗在效果获益上不仅没有输于O药、K药,反而还具有一定的优势,这是十分令人欣喜的。
事实上,除了霍奇金淋巴瘤,信迪利单抗已经开始在其他癌肿中开展临床试验,大展拳脚,包括一线非鳞非小细胞肺癌、一线肺鳞癌、二线肺鳞癌、EGFR TKI治疗失败的EGFR突变阳性的非小细胞肺癌、一线胃癌、一线肝癌、一线食管癌、二线食管癌等。
目前,信迪利单抗在肺癌一线治疗方面的Ib期临床数据已公布,数据显示:
针对非鳞非小细胞肺癌,信迪利单抗+培美曲塞/顺铂的客观缓解率达到68.4%,
针对鳞状非小细胞肺癌,信迪利单抗+吉西他滨/铂类的客观缓解率达到64.7%。
今年ASCO大会上,公布了一项临床研究结果,该研究评估了信迪利单抗新辅助治疗中国可手术的肺鳞癌患者的安全性和疗效。
在22例肺鳞癌患者中,影像学评估显示:信迪利单抗新辅助治疗的客观缓解率为13.6%。安全性方面,在新辅助治疗期间出现的不良反应大多温和可控。
信迪利单抗目前正在多个癌肿中开展临床,虽然还没有获批肺癌相关适应症,但已公布的消息也向我们展示了它良好的发展前景,且由于信迪利单抗的大多临床试验是在中国患者中开展,相信这也会对中国患者更加有利。
2卡瑞利珠单抗

卡瑞利珠单抗是恒瑞医药自主研发并具有知识产权的人源化PD-1单克隆抗体,可与人 PD-1 受体结合并阻断 PD-1/PD-L1 通路,恢复机体的抗肿瘤免疫力,从而形成癌症免疫治疗基础。
2019年5月5日,卡瑞利珠单抗正式获批上市,适用于至少经过二线系统化疗的复发或难治性经典型霍奇金淋巴瘤患者的治疗,即获批用于三线治疗。
临床研究数据显示:
在既往接受过至少二线系统性治疗的复发/难治性经典霍奇金淋巴瘤患者中,评估发现,卡瑞利珠单抗的客观缓解率(ORR)达84.8%,完全缓解(CR)率达30.3%,且安全性可控。
如此高的客观缓解率,那么特瑞利珠单抗对比O药、K药在霍奇金淋巴瘤中的效果如何?
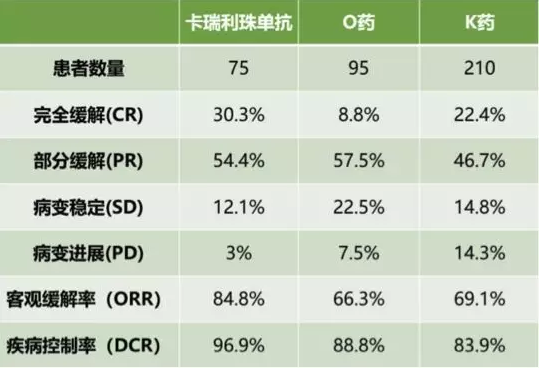
(图片来源:瑞德生健康网)
综合上表数据,在霍奇金淋巴瘤的治疗上,卡瑞利珠单抗的疗效优于O药、K药。
除了在霍奇金淋巴瘤中的临床数据,卡瑞利珠单抗也已经在非小细胞肺癌、肝癌、食管癌、鼻咽癌等多个癌肿中开展了临床。
根据公开发表的数据:
卡瑞利珠单抗联合阿帕替尼治疗二线及以上EGFR和ALK野生型晚期非鳞非小细胞肺癌的/Ⅱ期临床研究结果显示:联合治疗的总体缓解率(ORR)为30.8%,中位无进展生存期(PFS)为5.9个月,且在血液肿瘤突变负荷高的患者中这一联合疗效更优,ORR为52.6%,中位PFS延长至7.8个月。
卡瑞利珠单抗二线及以上治疗晚期肝细胞癌的II期研究结果显示:单药治疗ORR为13.8%,6个月总生存率(OS)为74.7%。
卡瑞利珠单抗二线治疗鼻咽癌的研究结果显示:单药治疗ORR为34%,联合化疗方案一线治疗鼻咽癌的ORR达91%。
卡瑞利珠单抗单药二线治疗食管鳞癌的III期临床研究结果显示:对既往一线化疗失败的晚期或转移性食管鳞癌患者,接受卡瑞利珠单抗单药治疗对比化疗,可显著延长患者的生存期。
3特瑞普利抗(拓益®, JS001)
制药公司:上海君实生物
拓益®(特瑞普利单抗)是一种针对各种恶性肿瘤的重组人源化抗PD-1注射用单克隆抗体,是国内第一个具有自主知识产权的PD-1单抗,与K药和O药相比,它具有更高的亲和力,能够结合PD-1,强效阻断PD-1通路,提高抗肿瘤疗效。
2018年12月17日,特瑞普利单抗的上市申请正式获得国家药品监督管理局批准,用于治疗标准治疗失败后的局部进展或转移性黑色素瘤。
其研究结果显示:在既往接受过全身系统性治疗失败的不可切除或转移性黑色素瘤患者中,特瑞普利单抗的客观缓解率(ORR)为17.3%, 疾病控制率(DCR)达57.5%,1年生存率为69.3%。
对比K药疗效,结果如何?
根据K药在中国的一项开放性研究的公开数据显示:在转移性黑色素瘤患者中,K药的客观缓解率为16.7%,疾病控制率为38.2%,1年生存率为50.8%。
可见,特瑞普利单抗在黑色素瘤患者中的疗效从目前来看是不输K药的。
除了已经获批的黑色素瘤适应症,君实生物公司正与中国众多临床试验中心的KOL及PI合作,进行包含恶性黑色素瘤、尿路上皮癌、胃癌、食管癌及鼻咽癌等肿瘤适应症的特瑞普利单抗(JS001 )II期和III期临床试验。

(图片来源:君实官网)
以上是特瑞普利单抗在其他多个癌肿中的临床试验数据,可以看到特瑞普利单抗在诸多癌肿中均显示出了不错的疗效和前景,并且根据公开数据显示,在安全性上,特瑞普利单抗也表现不错,不良反应大多安全可控。
作为我国首个具有自主知识产权的PD-1药物,特瑞普利单抗凭借不俗表现频频亮相国际各大会议,向世界展示了中国的药物创新研发能力。
值得一提的是,根据近期数据,特瑞普利单抗在尿路上皮癌及黑色素瘤等的临床研究中展现了不输于甚至优于国内外同类产品的良好表现,我们期待该药在中国能获批更多适应症,帮助更多中国患者从中获益。
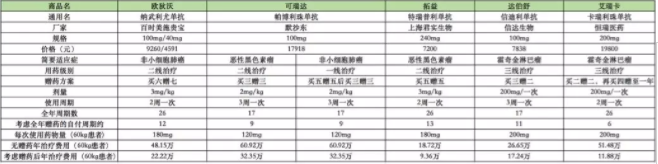
以上为已在国内上市的三大国产PD-1,从疗效数据看,三大药物均不逊色于“免疫神药”O药、K药,而且非常重要的是,除了卡瑞利珠单抗的定价较高,在价格上,国产PD-1相较于O药、K药具有非常明显的价格优势。
即使大家看到卡瑞利珠单抗的定价高,但加上现有的赠药政策,患者实际承担的费用还是要远低于O药、K药的。
总体来说,已上市的国产PD-1,除了卡瑞利珠单抗,即使患者是全自费,总体费用也远低于O药和K药,不得不说,有了高效的国产PD-1的竞相上市,确实能够惠及到更多的中国患者。
这里还要提到,目前的几款国产PD-1药物的适应症不包括肺癌,也就是说肺癌患者使用这几类药物是不能享有赠药政策的,所以,肺腾在这里也非常希望国产药物的肺癌临床研究能尽快推进,肺癌适应症能尽快审批,让广大肺癌患者也能享受到赠药政策。
除了以上已经上市的三大国产PD-1,这里还需要提到一个正在上市申报审批阶段的国产PD-1,那就是百济神州的替雷利珠单抗(BGB-A317)。
4替雷利珠单抗(BGB-A317)
制药公司:百济神州

(图片来源:百济神州官网)
替雷利珠单抗是百济神州一款在研的人源化IgG4单克隆抗体,对PD-1具有高亲和力和特异结合性。
一项评估替雷利珠单抗联合含铂类双药一线治疗晚期NSCLC和SCLC的疗效及安全性的II期临床研究(BGB-A317-206)显示:在54例接受了替雷利珠单抗治疗的患者中,总体疾病控制率(DCR)达91%。
一项针对不可耐受标准治疗或标准治疗失败的晚期或转移性鼻咽癌患者的I/II临床研究(BGB-A317-102)结果显示:21例可评估患者中,总ORR为43%,DCR为86%,中位PFS为10.4个月。
等等数据均展现了替雷利珠单抗在晚期实体瘤患者中的良好耐受性和抗肿瘤活性。
目前替雷利珠单抗申报审批的适应症为复发/难治性霍奇金淋巴瘤以及局部晚期或转移性尿路上皮癌的二线治疗,期待今年能够听到这一国产PD-1获批的好消息。
除了上述国产PD-1外,目前至少还有十多家药企摩拳擦掌,准备加入PD-1/PD-L1的研发阵营,从某种程度上来说,这体现了我国药物研发能力的提高,从另外一种程度上来说,如果当前研发的PD-1/PD-L1在疗效上能达到K药、O药的水平,并且在适应症上能够更大范围地涵盖更多的癌肿,相信对于广大肿瘤患者,这一定是一件值得期待并且骄傲的事情。
此外,从现有上市的PD-1情况来看,在价格层面上国产药物相较于高价的国外药物,一定程度地减轻了患者的家庭负担,至于未来更多药物的出现是不是能够更进一步地促使这类药物以更低价格面向更多的患者,暂时不知,但希望如此。